In natuurlijke zuivere wateren heerst een stabiel biologisch evenwicht. Verschillende planten, plankton, vissen en micro-organismen zijn via het zogenaamde voedselnet van elkaar afhankelijk (zie punt 7). Elke ingreep van buitenaf op een van de leden van de keten heeft onvermijdelijk een invloed op alle organismen van dit ecosysteem. Een natuurlijk ecosysteem is binnen bepaalde grenzen in staat om storingen op te vangen. Kunstmatige ecosystemen, zoals bijv. vijvers met een kunstmatige visstand, kunnen zelfs door kleine verstoringen voor lange tijd hun biologisch evenwicht verliezen.
De meeste problemen in een tuinvijver zijn te wijten aan een te hoge visstand en het voederen van de vissen. Door de geringe oppervlakte van tuinvijvers kunnen overtollig visvoer en uitwerpselen van de vissen zonder hulp niet blijvend afgebroken worden. Door kunstmatige voeding toe te voegen heeft de mens ingegrepen in het biologische evenwicht. De toestand van overbemesting die daaruit voortvloeit, door experts ook eutrofiëring genoemd, leidt tot algengroei en grasgroen water en vertroebelt – letterlijk – de vreugde van de eigenaar van een tuinvijver.
In het begin heeft dit geen negatieve invloed op de organismen in de vijver. De algen produceren tijdens hun groei zuurstof die dan in het water wordt afgegeven. Na een paar dagen of weken sterven de algen af en zinken ze naar de bodem. Terwijl ze zinken en wanneer ze op de bodem liggen worden ze door plankton en micro-organismen (bacteriën en schimmels) verteerd. Deze organismen nemen slechts een klein deel van de voedingsstoffen in hun eigen biomassa op, de rest wordt afgegeven in het omringende water. Het totale afbraakproces wordt mineralisatie genoemd.
Tijdens de mineralisatie wordt echter evenveel zuurstof gebruikt als de algen voordien hebben geproduceerd. Het zuurstofgehalte in het water neemt snel af zodat vissen en andere waterorganismen stikken. Op dat moment is het evenwicht in de tuinvijver zodanig verstoord dat het niet meer vanzelf kan herstellen.
Om te vermijden dat vissen sterven tengevolge van zuurstoftekort, worden vaak circulatiepompen of fonteinen gebruikt om het water met zuurstof te verrijken. Maar wanneer van buitenaf zuurstof wordt toegevoegd, kan alleen worden verhinderd dat vissen sterven. Het water blijft echter troebel en behoudt zijn ongewenste groene kleur. In de volgende hoofdstukken worden de afzonderlijke factoren die dit proces veroorzaken en versnellen, uitvoeriger beschreven en wordt de werking van de Biotec-filter uitgelegd.
Het zuurstofgehalte
Bijna alle organismen hebben net zoals de mens zuurstof nodig om te ademen. Organismen die op het land leven, kunnen enkel zuurstof uit de lucht halen. Normaal gezien bevat de lucht meer dan genoeg zuurstof (ca. 21%). Daartegenover beschikken de bewoners van tuinvijvers enkel over de zuurstof die in het water is opgelost, dat zelden waarden van meer dan 12 mg/l bereikt. Deze waarde komt overeen met ca. 0,0012% van het totale gewicht. In vergelijking met de lucht, die bijna voor 1/5 uit zuurstof bestaat, is dat extreem weinig. Daarom is het voor alle bewoners van tuinvijvers van levensbelang dat het water zoveel mogelijk met zuurstof wordt verzadigd.
Het zuurstofgehalte van het water hangt af van verschillende factoren. Verbruikte zuurstof kan enkel vervangen worden door zuurstof uit de lucht of door zuurstof die vrijkomt via fotosynthese van planten en algen. Dit laatste is echter alleen mogelijk indien er voldoende licht is.
Temperatuur, luchtdruk en vooral de grootte van het wateroppervlak in verhouding tot het watervolume beïnvloeden de opname van zuurstof uit de lucht in het water.
Het hangt onder andere van de temperatuur af of de zuurstof oplost in het water (zie tek. 1). Bij hoge temperaturen zoals bijv. in de zomer lost minder zuurstof op dan bij lagere temperaturen. Terzelfder tijd hebben organismen, naarmate het in hun omgeving warmer is, steeds meer zuurstof nodig. Algemeen geldt dat de snelheid van metabolische reacties en dus ook het zuurstofverbruik verdubbelt wanneer de temperatuur 10 graden stijgt (tek. 2). Daarom kan er bij hoge temperaturen gemakkelijk zuurstof te weinig zijn.
Het zuurstofgehalte in tuinvijvers is onderhevig aan sterke schommelingen. Dit is o.a. te wijten aan het feit dat planten en algen die overdag zuurstof produceren, ’s nachts van de omzetting van ‘zonne-energie’ omschakelen op verbranding (ademhaling) en daarbij zuurstof nodig hebben. ’s Nachts kan daardoor zodanig veel zuurstof worden verbruikt dat alle zuurstof die in het water was opgelost nog vóór zonsopgang is opgebruikt. Deze wijziging van het zuurstofgehalte wordt dag- en nachtschommeling genoemd. Daardoor is het leven van de vissen en de andere ademende organismen vooral in de vroege morgen in gevaar. Men mag dan ook aannemen dat het niet zinvol is ’s nachts ventilatiesystemen uit te schakelen.
Wanneer er in het water te veel voedselbestanddelen zijn door afgestorven algen- en plantendeeltjes of overvloedig visvoer, verbruiken de micro-organismen bovendien – vooral in warm water – een enorme hoeveelheid zuurstof. Dit verbruik kan zo hoog zijn dat er niet genoeg zuurstof overblijft voor vissen en andere dieren. Ze sterven en de vijver verandert in enkele uren in een stinkende smurrie : Het biologische evenwicht is verstoord, de vijver ‘slaat om’.
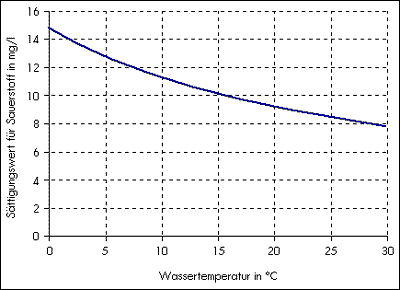
tek. 1: verzadigingswaarden (100 %) voor zuurstof, afhankelijk van de temperatuur
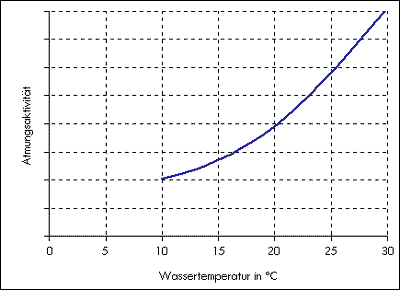
tek. 2: ademactiviteit naargelang van de temperatuur
De PH waarde
De pH-waarde van het water is één van de belangrijkste factoren voor alle organismen in het water. Ze overleven enkel geringe schommelingen van de pH-waarde.
De pH-waarde is een maat die de concentratie van een zuur of een loog aangeeft. Ze wordt in een schaal van 0 tot 14 ingedeeld. Zuiver water is met een pH-waarde van 7 neutraal, bij leidingwater ligt de pH-waarde normaal gezien tussen 7,0 en 8,0.
Alkalische oplossingen hebben een pH-waarde van meer dan 7. Hoe hoger de pH-waarde boven 7 ligt, hoe alkalischer de oplossing is. In het huishouden worden bijv. zeepoplossingen gebruikt met een pH-waarde van ca. 10.
Bij zure oplossingen ligt de pH-waarde onder 7. Hoe lager de pH-waarde onder 7 ligt, hoe sterker het zuur is. Een voorbeeld van een sterk zuur is zoutzuur met een pH-waarde van minder dan 1. Ook dranken met koolzuur zijn zure oplossingen.
Optimaal voor veelsoortig leven in tuinvijvers zijn pH-waarden tussen 6 en 8,5. Een pH-waarde buiten deze grenzen kan bij vissen leiden tot schade aan huid en kieuwen en in extreme gevallen zelfs tot de dood.
Chemisch gezien is de formule voor water H2O. Dat betekent dat elke molecule water twee atomen waterstof (H) en één atoom zuurstof (O) bevat. Deze waterstofmoleculen bestaan uit hydroxide-ionen met een negatieve lading (OH-) en waterstofionen met een positieve lading (H+). De som van beide geeft dus een neutraal molecuul. De definitie van de pH-waarde werd verbonden met de concentratie van de waterstofionen. Om niet met onpraktische getallen te moeten werken, werd de pH-waarde als negatief logaritme van de concentratie van de waterstofionen gedefinieerd. Wanneer de concentratie van de waterstofionen bijv. 0,01 mol/l (= 10-2 mol/l) bedraagt, heeft de betreffende oplossing een pH-waarde van 2. Hoe hoger de concentratie van de waterstofionen, hoe lager de pH-waarde. Wanneer de pH-waarde bijv. daalt van 7 naar 6, stijgt de concentratie van de waterstofionen tienvoudig.
Het kooldioxide- en kalkgehalte
Het kooldioxidegehalte van het water hangt net zoals het zuurstofgehalte af van verschillende factoren. Onder andere via het wisselsysteem met de lucht wordt kooldioxide opgenomen en afgegeven. De ademhaling van alle organismen in het water is een extra bron van kooldioxide. (zie tek. 5 onder punt 6).
Planten en algen hebben voor hun fotosynthese kooldioxide nodig. Die halen ze overdag uit het water. Het kan gebeuren dat er zoveel kooldioxide verbruikt wordt, dat de pH-waarde in wateren die slecht belucht zijn, meetbaar stijgt. Daarbij kunnen pH-waarden van meer dan 8,5 worden bereikt. ’s Nachts produceren ook de planten en algen kooldioxide, met als gevolg dat de pH-waarde opnieuw daalt.
Kooldioxide lost aanzienlijk gemakkelijker op in water dan in zuurstof omdat het samen met water het goed oplosbare koolzuur vormt:
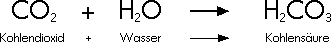
Daarnaast komt het ook voor als calciumwaterstofcarbonaat in gebonden vorm:
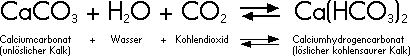
Kooldioxidehoudend water kan dus door een chemisch proces kalk – wetenschappers noemen dit calciumcarbonaat – oplossen. De twee pijlen wijzen erop dat de reactie in beide richtingen mogelijk is. Wordt kooldioxide uit het water gehaald, dan vormen zich ongebluste kalk en kooldioxide tot het evenwicht opnieuw hersteld is. Ongebluste kalk herkent men aan een witte neerslag die algemeen gekend is als ketelsteen. Aangezien water, wanneer het verhit wordt, niet meer in staat is om kalk in opgeloste vorm vast te houden, slaat de kalk neer in de vorm van ketelsteen. Het kalkgehalte van het water beïnvloedt de pH-waarde, m.a.w. het bepaalt of het water neutraal, zuur of basisch reageert. Hoe groter de concentratie aan opgeloste kalk, hoe meer kooldioxide gebonden wordt in de vorm van koolzuurhoudende kalk – wetenschappers noemen dit calciumwaterstofcarbonaat – en hoe minder koolzuur dus vrij in het water aanwezig is. De pH-waarde ligt daardoor veeleer tussen neutrale en licht basische waarden. Daarentegen zorgt het vrije koolzuur – zoals de naam reeds aangeeft – ervoor dat de pH-waarde daalt en de oplossing veeleer zuur wordt.
De beschikbare voedingsstoffen
Algemeen
Alle organismen hebben voedingsbestanddelen nodig voor hun energiewinning en hun bouwstofwisseling. Met bouwstofwisseling wordt de algemene groei bedoeld. De groei van alle organismen in de tuinvijver hangt af van verschillende factoren. Is één van deze factoren niet voldoende beschikbaar, dan wordt de groei begrensd. Men spreekt dan van een ‘limiterende factor’. Deze limiterende factor is voor de vissen, waterplanten, algen en micro-organismen in de tuinvijver telkens verschillend:
– Vissen en dieren hebben een hoogwaardige voeding nodig die rijk is aan energie en voedingsstoffen (bijv. insecten, visvoer, enz.) en die terzelfder tijd de groei beperkt.
– Waterplanten hebben voedingsstoffen, kooldioxide en licht nodig. Zij kunnen het nodige voedsel uit het water of uit de bodem halen. Het licht speelt hier een groeibeperkende rol.
– Algen hebben dezelfde basisbehoeften als waterplanten. Met uitzondering van de draadalgen kunnen zij echter enkel de voedingsstoffen gebruiken die in het water zijn opgelost. Normaal gezien beperkt het voedingsstofgehalte van het water de groei.
– Micro-organismen verteren tijdens de mineralisatie dode organische biomassa. De voedingsstoffen zijn onmiddellijk uit de biomassa of uit het water afkomstig. Het energiegehalte en de beschikbaarheid van dode biomassa spelen hier een groeibeperkende rol.
Tijdens de stofwisseling worden tussen- en eindproducten gevormd die dan gedeeltelijk als voedingsstoffen in het water worden afgegeven. Stikstof (ammonium of ammoniak, nitraat, nitriet) en fosfor (fosfaat) zijn de belangrijkste voedingsstoffen. De beperking van de natuurlijke groei van de algen door het voedingsstofgehalte van het water wordt opgeheven door het toevoegen van extra voedingsstoffen, zoals bijv. visvoer. Dit leidt tot de gekende hierboven beschreven nadelen.
Ammonium en ammoniak
Ammonium is de eerste anorganische stikstofverbinding die ontstaat bij de afbraak van eiwit. Het ammonium- en ammoniakgehalte is van belang omdat ammoniak zeer giftig is voor vissen.
Ammonium en ammoniak houden elkaar in evenwicht:
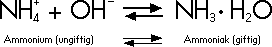
Dit evenwicht hangt af van de pH-waarde van het water. Wanneer de pH-waarde stijgt, verschuift het zwaartepunt naar de giftige ammoniak. Bij een pH van bijv. 7 bedraagt de verhouding ammonium : ammoniak 99 : 1. Stijgt de pH tot 9, dan wordt de verhouding 70:30. Hoe hoger de pH-waarde, hoe kritischer hoge ammonium- en ammoniakgehaltes worden voor de fauna in de tuinvijver.
Micro-organismen zorgen ervoor dat het water van ammoniak, ammonium en nitriet wordt ontdaan. Dit proces wordt nitrificatie genoemd (tek. 4 onder punt 5). Het afbraakproces gebeurt in twee fases die telkens door verschillende micro-organismen worden uitgevoerd.
In een eerste fase worden ammoniak en ammonium afgebroken tot nitriet. Deze oxidatie gebeurt door bacteriën die “nitrificanten van de eerste orde” worden genoemd. In de tweede fase wordt het nitriet door andere micro-organismen – “de nitrificanten van de tweede orde” – tot nitraat afgebroken. Bij beide oxidatieprocessen halen de bacteriën de nodige zuurstof uit het water. De eerste fase van de nitrificatie verloopt trager dan de tweede omdat de nitrificanten van de eerste orde slechts traag groeien.
Nitriet (NO2)
Tijdens de nitrificatie, die een watertemperatuur van minstens 10°C vooropstelt, wordt ammonium door speciale micro-organismen eerst tot nitriet en vervolgens tot nitraat afgebroken (tek. 4, p. 8). Nitriet ontstaat bij dit proces als tussenproduct. Vanaf een concentratie van 0,2 mg/l is nitriet giftig voor vissen. Wanneer het door de voorhanden zijnde micro-organismen echter onmiddellijk verder wordt afgebroken tot nitraat, bestaat er geen gevaar voor de visstand.
Nitraat (NO3)
Nitraat is het voorlopige eindproduct van de afbraak van eiwit. Het ontstaat door de trapsgewijze afbraak van ammonium via nitriet (tek. 4, p. 8). Bij de nitrificatie wordt nitraat gevormd door de afbraakprestaties van de nitrificanten van de tweede orde (micro-organismen). Nitraat is in tegenstelling tot ammoniak en nitriet niet giftig voor vissen. Het vormt dan ook geen directe bedreiging voor de visstand.
Nitraat is veeleer een meststof die de groei van de planten stimuleert. Een stijging van het nitraatgehalte heeft automatisch een sterkere plantengroei tot gevolg. Het resultaat daarvan is een vertroebeling van de vijver door algengroei. Daardoor wordt het biologische evenwicht verstoord. De afgestorven algen zinken naar de bodem en worden daar door de micro-organismen afgebroken. Deze gebruiken daarbij grote hoeveelheden zuurstof. Tijdens dit afbraakproces komen nitraten vrij die voordien in de plantaardige cellen opgenomen waren. Dit veroorzaakt opnieuw een sterkere algengroei. Dit proces kan enkel afgebroken worden wanneer de micro-organismen de voedingsstoffen omzetten in eigen biomassa of in stikstof in de lucht, die niet bruikbaar is voor planten.
Een andere bacteriëngroep, de denitrificanten, zorgt ervoor dat het nitraat verder wordt omgevormd tot stikstof in de lucht. Met denitrificatie bedoelt men de afbraak van nitraat via nitriet (nitriet blijft in gebonden toestand en komt niet vrij) tot gasvormige stikstof (tek. 3). Gasvormige stikstof is chemisch stabiel en is niet meer bruikbaar voor bio-organismen. Door de denitrificatie wordt de kringloop van nitraatproductie en -verwerking doeltreffend onderbroken. Denitrificatie komt enkel voor in een zuurstofarme omgeving.
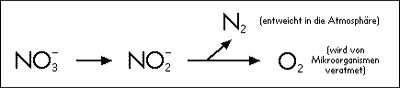
Tek. 3: vereenvoudigde voorstelling van denitrificatie.
De koolstofkringloop
De fotosynthese
Fotosynthese is de bestaansvoorwaarde voor alle levende wezens. Het vormt daardoor het belangrijkste biologische proces op aarde. Alle groene planten en enkele bacteriën doen aan fotosynthese om biomassa op te bouwen die dan als voedsel door andere organismen kan worden gebruikt. Tijdens de fotosynthese wordt anorganische kooldioxide omgevormd tot organische biomassa (tek.5).
Organismen die aan fotosynthese doen, voorzien in hun energiebehoefte door zonlichtenergie op te nemen en om te vormen. Andere levende wezens, zoals bijv. alle dieren en de mens, moeten voedsel opnemen om te kunnen voorzien in hun energie- en koolstofbehoeften.
Fotosynthese maakt het voor planten en algen mogelijk om te groeien zonder “brandstoffen” te verbruiken. Daarbij nemen ze voedingsstoffen op en geven ze zuurstof in het water af.
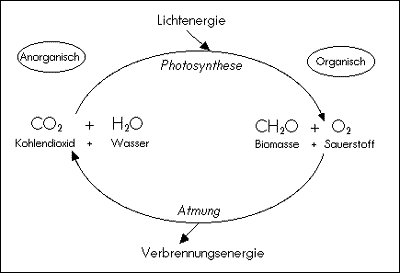
Tek. 5: voorstelling van fotosynthese en ademhaling (verbranding)
De ademhaling
Door te ademen (stofwisseling) kunnen organismen vreemde biomassa (voeding) en zuurstof omzetten in kooldioxide en water, waardoor ze energie winnen. Kooldioxide en water worden hierbij uitgescheiden, ze worden bij wijze van spreken ‘uitgeademd’.
Fotosynthese en ademhaling vormen een gesloten kringloop (zie tek. 5). Groene planten kunnen deze kringloop volledig doorlopen. Overdag doen ze aan fotosynthese – het zonlicht levert hen daarbij energie – en bouwen ze organische biomassa op. Zuurstof vormt hierbij een afvalproduct dat aan de omgeving wordt afgegeven. ’s Nachts schakelen ze hun stofwisseling om en putten ze uit hun energiereserves terwijl ze zuurstof verbruiken.
Al de andere organismen kunnen slechts een deel van de koolstofkringloop uitvoeren. Ze zijn niet in staat om aan fotosynthese te doen. Ze nemen energierijk voedsel op en zetten dit om in organische biomassa. Dit proces wordt ademhaling genoemd. Hierbij wordt zuurstof verbruikt en kooldioxide uitgescheiden.
De voedselpiramide en het voedselnet
De organismen in een tuinvijver zijn met elkaar verbonden via veelsoortige relaties (tek. 7). Planten en algen vormen als producent de voedselbasis voor het ecosysteem ’tuinvijver’. Ze worden opgegeten door plankton, die op hun beurt worden opgegeten door iets grotere organismen. Vissen voeden zich met deze kleine organismen en plankton of met de daaropvolgende leden van de voedselketen. Onder de vissen zijn er ook zuivere planteneters. De uitwerpselen van vissen, afgestorven plankton en stukken van planten worden door bodemorganismen verder omgezet en uiteindelijk door de micro-organismen gemineraliseerd. Bij de mineralisatie worden organische verbindingen ‘geoxideerd’ en tegelijkertijd komen ook voedingsstoffen vrij zoals nitraat of fosfaat. Deze voedingsstoffen staan dan op hun beurt ter beschikking van de planten en algen voor hun groei.
Op die manier is de cirkel volledig gesloten. Hij toont heel duidelijk hoezeer de afzonderlijke organismen op elkaar aangewezen zijn. Die verbinding wordt ook voedselketen of nog beter voedselnet genoemd. De stabiliteit van het voedselnet is doorslaggevend voor het biologische evenwicht. Hoe meer verschillende soorten er voorkomen, hoe stabieler het voedselnet is en dus ook het volledige ecosysteem. Wordt er van buitenaf ingegrepen in een deel van het voedselnet, dan heeft dat een uitwerking op alle organismen.
Aangezien bij het ‘eten’ en ‘gegeten worden’ telkens energie- en stofverliezen tot 90% optreden, wordt de voedselketen vaak voorgesteld als piramide (tek. 6). Een eenvoudig voorbeeld moet dit verband verduidelijken: met 100 kg sojameel kan men 10 kg varkensvlees produceren, dat dan kan worden gebruikt voor consumptie door de mens. Wanneer de mensen zich direct zouden voeden met sojameel, dan zouden ze maar 1/10 nodig hebben van het sojameel dat gebruikt wordt bij de vleesproductie.
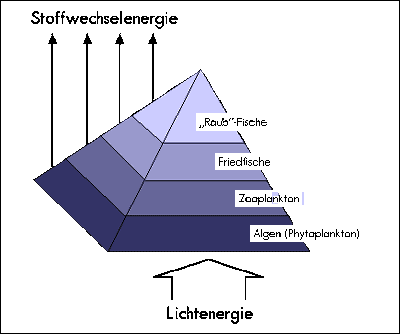
Tek. 6 De voedselpiramide
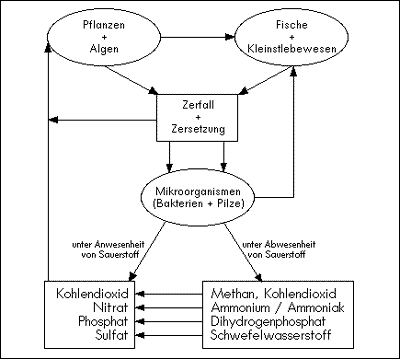
Tek. 7 Afbraak en kringloop van de stoffen in het water

Tek. 4 vereenvoudigde kringloop van stikstof

